国試対策の講義を行った。ほとんどの学生がよく理解できていないと思われる酸塩基平衡だ。国試対策だから4年生だ。
CO2+H2O<=> H2CO3<=> HCO3-+H+
が生体内で酸塩基平衡を保つ重要な反応式だ。この右から左あるいはその逆の反応へは生体内では炭酸脱水酵素が100万倍にスピードアップさせるといわれている。つまり下図のように代謝の結果できた二酸化炭素を血液に炭酸水素イオン(重炭酸イオン)として溶かし、肺では逆に二酸化炭素ガスにして排出する速度を高めている。ドライアイスをコップの水に突っ込んでも生じる反応の速度を促進する酵素だ。
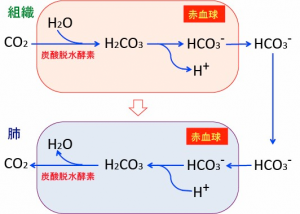
http://blog.goo.ne.jp/kfukuda_ginzaclinic/e/b8226560d6717ec7fd57eca02983fa82から拝借しました
肺にこの酵素があるのは上記の理由だし、腎臓では血液に溶けている重炭酸イオンは濾過されて尿へ排出されちゃうところ、この酵素で二酸化炭素にして細胞内に再吸収するので、腎臓にも大量にこの酵素がある。
血液のpHは 7.40 ± 0.05 と厳密に保たれている。あなたが肉をたらふく食べたって血液は酸性にならないし、ベジタリアンの血液だってpHはこの範囲にある。つまりこの血液pHを一定に保つ仕組みがあるのだ。
この仕組を理解する上で、上記の反応式が重要なのだ。血液の水素イオン濃度が高くなったとき、上の式が右から左に反応し二酸化炭素を肺からより多く捨てれば水素イオン濃度が高くなることがない=pHが一定に保たれるわけだ。他にも腎臓の働きもあるので、これを解説したのだ。
アシドーシスとアシデミア、アルカローシスとアルカレミアの違いとかだな。
で一通りの解説が終わって、質問を受付たのだが、「炭酸水素イオン(重炭酸イオン)が分からない」という質問が来て、答えられなかった。
炭酸水素イオンの何が分からないのか、こっちが分からないから聞いたのだが、何か分からないのかが分からない。いつものことだ。
なんと説明したらいいのか…答えられなかった。
炭酸水素イオンは高校の化学基礎で、ひょっとしたら中学の理科でもでてくると思うところですが…
そんでもって、昨日は非常勤の方の大学で、研究室の卒研生の中間発表の練習を聞いたのだが、あまりにも差が大きいので、とほほと ため息だったのだ。
ん~、小生の昭和時代では中学・高校(化学Ⅰ、Ⅱ)で習った記憶がありません。
一通り、ネットで調べてみましたが、現在でも教科書レベルでは
CO2 + H2O → H2CO3(ないし2H(+)CO3(2-))
までで、参考書の脚注にかろうじてH2CO3のほとんどは
H(+) + HCO3(-)
にすぐ電離して水溶液中に存在しているとある。反応速度を議論しなければならない場合にはじめて炭酸水素イオンに着目しなければならなくなるから、中高生ではきびしいかもしれませんな。
イオン化傾向なども反応論抜きで教えているから「暗記項目」になってしまい、「なぜ」を知りたい生徒の化学離れを招いている感じがする。
じゃあ、どう教えるのか。
水にとけた二酸化炭素が炭酸になり、炭酸が水素イオンと炭酸水素イオンに電離するところまでは上記参考書の説明を拝借して、そこからふたたび二酸化炭素が放出されるところは、なじみの深い炭酸飲料を例にとって、口の中でシュワ~ってなるのは唾液にこの酵素が含まれていて、酵素のくぼみがHCO3-のCO2の部分を捕まえてもぎとっているのだ、という感じでしょうか?
科学印刷業者さ
コメントありがとうございます。
どうやら中学では炭酸水素ナトリウムはでてくるようで、加熱すると二酸化炭素がでてくるよ というようなことのようですね。
この重炭酸緩衝系は呼吸の二酸化炭素運搬でキモとなる反応式なわけで1年生の生理学で既に学習しています。それが4年生になって炭酸水素イオンがわからないといわれると、何がどのようにわからないのか、勿論、聞いてもわからないわけで、途方にくれちゃったわけです。
馴染み深い炭酸飲料で思い出したのですが、ガスの水への溶解度は温度が高い程少ない。コップに入れたコーラを温めると泡がでてくるでしょ。と温度ー酸素溶解度曲線のグラフを見せて、夏場、金魚が水面でプカプカするのは何故?とか説明したのですが、彼らの頭には水に「モノ」を溶かすのは温度が高い方がいいという固定概念でコチコチで、試験に出すと正解率は50%なのです。動物がヘモグロビン・ヘモシアニンを進化の途上で開発し生存に有利になった理由を説明したのですが、へ~という言葉もないのです(http://seigi.accsnet.ne.jp/sigh/blog/?p=7539)。
「モノを溶かすのは温度が高い方がいいという固定概念」を除いて「気体は温度が低い方が液体に溶けやすい」という概念を読者に理解してもらうのにウチが作った挿絵の話をいたしましょう。
個体分子はプルプル振動しているけれど分子間力で互いに寄り集まっている○(中に顔が描いてある)、液体分子は泳ぎ回っている○、気体分子は飛び回っている○で、それぞれの○は温度が高くなると運動性(元気さ)が高まる。泳ぎ始める温度、飛び始める温度はそれぞれの分子の種類によって異なるので、同じ温度でも個体のもの、液体のもの、気体のものがある。
ここでそんな「元気さ」が異なる分子が混ざり合う「なじみやすさ」を「溶解度」と呼ぼう。
個体分子は温度が高くなって元気が出てくると「泳げるかも!」となって、液体分子となじみやすくなり、温度が下がって元気がなくなってくると「じっとしとくわ」となって沈殿する。気体分子は温度が低くなると「飛ぶのしんどいからちょっと泳いでくるわ」となって液体分子となじみやすくなり、温度が上がって元気が出てくると「のろのろ泳いでいられるか、自由に飛びまわるんだ!」とばかり液体から飛び出していく・・・
って挿絵になりました。
ヘモグロビンはさしずめ暴れん坊の酸素分子を「君の活躍する場所はここじゃないんだ、そこまでつれていく」って言ってしっかり抱きかかえていく絵になりましょうか。
文字列だけでは日曜の夕食で飲んでる私の理解がいまいちなので、あとでイラストに変換してみます。ありがとうございます。
漫画生理学をこ試みたことがあるのですが、当方とイラストレータのコミュニケーションがうまくいかず、失敗でした。時間制限があったからです。自分でイラストを描けばいいのですが、イラストにすると、単純すぎることになりがちで、正確性に欠る・誤解されやすい とかを考えているといつまでたっても終わらない。
小学生じゃあるまいし… と思うのが間違いで、小学生にもわかるような説明でないといけないんですよね。